Bs Nguyễn Duy Phi Hiệp - Khoa Ung bướu
10.Điều trị:
Liệu pháp xạ trị
Trong hai thập kỷ qua, liệu pháp xạ trị đã phát triển thành một kỹ thuật đòi hỏi nhạy bén trong cả việc đánh giá sinh học khối u lẫn vật lý xạ trị. Việc sử dụng CT để mô phỏng và kỹ thuật ba chiều cho lập kế hoạch điều trị đã cải thiện độ chính xác trong thiết kế trường chiếu dựa trên sự hiểu biết về kích thước của khối u thông qua tia X. Kỹ thuật IMRT đã giúp giảm độc tính tại mô bình thường trong khi vẫn duy trì liều cao đến thể tích bia đích. Lợi ích của những tiến bộ này đã được chứng minh bằng sự cải thiện kiểm soát bệnh tại chỗ và giảm độc tính đối với mô bình thường. Ngoài ra, về mặt lý thuyết , bức xạ sử dụng các hạt tích điện, như proton hoặc ion carbon, không phải là các photon thông thường, có lợi thế trong việc tránh các mô bình thường nhạy cảm.
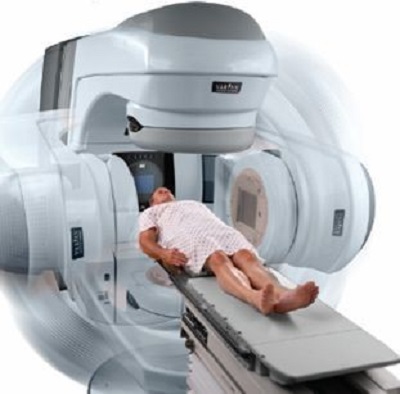
Những tiến bộ trong chẩn đoán hình ảnh đã góp phần cải thiện việc lập kế hoạch xạ trị. Cả PET và MRI đều cho phép mô tả khối u tốt hơn. Công nghệ hiện tại cho phép hợp nhất các hình ảnh từ các kỹ thuật hình ảnh khác nhau trên mỗi bệnh nhân để bác sĩ ung thư có thể xác định khối u và cấu trúc bình thường quan trọng chính xác hơn. Trong khi mục tiêu của IMRT là cải thiện việc lập kế hoạch điều trị, mục tiêu của xạ trị hướng dẫn bằng hình ảnh (IGRT) là cải thiện độ chính xác của điều trị. IGRT liên quan đến hình ảnh giải phẫu của bệnh nhân và sự tương ứng với vị trí bệnh nhân khi bệnh nhân được định vị trên máy xạ trị, với mục tiêu nhắm bia u chính xác hơn, giảm thiểu biến đổi liều điều trị và tránh các mô bình thường hiệu quả hơn. Theo cổ điển, xạ trị được phân phối ở mức 1,8 đến 2 Gy mỗi ngày trong tổng số 50 đến 70 Gy với việc giảm trường liên tiếp dựa trên đánh giá rủi ro. IMRT cho phép tích hợp tất cả các vị trí vào một kế hoạch duy nhất với khu vực có nguy cơ thấp nhận được liều thấp hơn trên mỗi phân liều trong khi khu vực có nguy cơ cao hơn nhận được liều cao hơn. Với kỹ thuật này, khối u thô thường được dùng liều hàng ngày cao hơn 2,1 Gy.
Hệ thống phân liều cải biên đã có những thành công nhất định. Chúng bao gồm tăng phân liều (1,2 đến 1,5 Gy hai lần hoặc ba lần mỗi ngày) và kỹ thuật tăng cường đồng thời (1,8 Gy vào buổi sáng cho toàn bộ trường chiếu theo sau là 1,5 Gy vào buổi tối đến trường chiếu nhỏ hơn bao gồm bệnh có nguy cơ cao). Với bất cứ kỹ thuật nào, điều cần thiết là duy trì 4 đến 6 giờ giữa các phân liều để cho phép mô bình thường được sữa chữa. Mặc dù thay đổi cách phân liều giúp cải thiện kết quả, nhưng lại gây nên sự gia tăng độc tính cấp mà không tăng những biến chứng về lâu dài. Tuy nhiên, kết quả sơ bộ của thử nghiệm giai đoạn III (RTOG 0129) so sánh phân liều tiêu chuẩn với hóa xạ trị phân liều gia tốc cho thấy không có sự khác biệt trong kết quả hoặc độc tính muộn giữa các nhóm. Bệnh ở giai đoạn đầu (T1, T2, N0) đáp ứng tốt với đơn trị bằng phẫu thuật hoặc xạ trị. Xạ trị cho phép bảo tồn cơ quan, bằng chứng là vai trò của nó trong việc quản lý bệnh ung thư giai đoạn đầu của dây thanh âm thanh quản và hầu họng. Tuy nhiên, bệnh tiến triển hơn (nói chung, giai đoạn III và IV) đòi hỏi phải phối hợp xạ trị với các phương thức khác.
Độc tính của xạ trị
Với những tiến bộ trong việc lập kế hoạch điều trị và phân phối bức xạ, độc tính liên quan đến bức xạ ít hơn hai thập kỷ trước. Độc tính bức xạ cấp tính nghiêm trọng phổ biến bao gồm viêm da, viêm niêm mạc, mất vị giác, khô miệng, chứng khó nuốt và rụng tóc. Giảm thính lực là không phổ biến. Khám nha và nhổ răng cần thiết nên được thực hiện trước khi xạ trị vì nhổ răng trong khi xạ trị có thể dẫn đến hoại tử xương. Bệnh nhân còn răng nên được dự phòng bằng fluoride. Bệnh nhân nhận được bức xạ có nguy cơ sâu răng cao do khô miệng gây ra bởi chấn thương tuyến nước bọt cũng như tổn thương niêm mạc. Phòng tia xạ bằng amifostine và pilocarpine không chứng minh được khả năng giảm khô miệng. Các kỹ thuật IMRT cho phép giảm liều đến các tuyến mang tai đã thành công hơn. Tương tự như vậy, rối loạn chức năng nuốt vĩnh viễn có thể tránh được bằng cách giảm liều xuống cơ hầu họng. Dự phòng, trước và sau điều trị bởi một nhà trị liệu về phát âm cũng giúp ngăn ngừa và giảm bớt chứng khó nuốt ở những bệnh nhân này.
Hóa xạ đồng thời
Hóa xạ trị đồng thời được sử dụng với mục đích bảo tồn cơ quan khi phẫu thuật sẽ dẫn đến tổn thương khả năng nói và nuốt. Hóa xạ đồng thời cũng được sử dụng ở bệnh nhân giai đoạn IVB khi mà phẫu thuật không được coi là lựa chọn tốt (bệnh nhân không đủ sức khỏe để phẫu thuật hoặc bệnh được coi là không thể phẫu thuật được, hoặc khi bệnh ở giai đoạn IVC, mặc dù chỉ là điều chị giảm nhẹ, nhưng mong muốn kiểm soát bệnh tại chỗ. Các nghiên cứu đã đánh giá việc hóa trị trước khi xạ trị hoặc phẫu thuật (tức là, tân bổ trợ hoặc hóa trị cảm ứng), thay vì phẫu thuật (tức là hóa xạ trị đồng thời) hoặc sau phẫu thuật(tức là hóa xạ trị bổ trợ). Cơ sở lý luận cho hóa xạ trị đồng thời dựa trên bằng chứng thực nghiệm về sự hiệp trợ giữa hóa trị và xạ trị, về mặt lý thuyết, bởi sự cản trở gián tiếp của hóa trị liệu và nhiều con đường gây đáp ứng stress do bức xạ nội bào liên quan đến quá trình chết theo chương trình, tăng sinh và sửa chữa DNA. Người ta đã phát hiện chắc chắn các tác nhân hóa trị liệu (ví dụ, cisplatin, 5-fluorouracil [5-FU], taxan và hydroxyurea) có thể gây ra tăng độ nhay phóng xạ và tăng tiêu diệt tế bào từ bức xạ. Cisplatin, thuốc được đánh giá rộng rãi nhất trong các thử nghiệm ngẫu nhiên lớn, có ưu điểm là không có độc tính là viêm niêm mạc; Tuy nhiên do là một chất tăng cường bức xạ, nó làm tăng độc tính viêm niêm mạc do bức xạ.
Xạ trị đồng thời với hóa trị liệu hoặc cetuximab đã được chứng minh là cải thiện khả năng sống sót ở bệnh nhân ung thư đầu và cổ. Các thử nghiệm lâm sàng ngẫu nhiên và phân tích tổng hợp cho thấy đối với ung thư tế bào vảy đầu và cổ giai đoạn tiến triển, hóa xạ trị đồng thời (với cisplatin) đem lại một lợi ích nhỏ nhưng thời gian sống còn cải thiện có ý nghĩa khoảng 8% sau 5 năm so với xạ trị đơn thuần. Các nhóm nghiên cứu ở Hoa Kỳ đã so sánh hóa xạ đồng thời với cisplatin ,liệu pháp xạ trị chia nhỏ với cisplatin và 5-FU, xạ trị đơn độc cổ điển ở bệnh nhân ung thư vảy ở đầu và cổ không thể cắt bỏ, cho thấy Cisplatin đồng thời ở mức 100 mg / m2 cứ sau 21 ngày với xạ trị hàng ngày (5 ngày mỗi tuần) tỷ lệ sống sót được cải thiện một cách có ý nghĩa. Điều trị đồng thời cisplatin với xạ trị cũng có liên quan với tỷ lệ bảo tồn thanh quản cao hơn trong ung thư thanh quản tiến triển tại chỗ, so với chỉ dùng xạ trị đơn độc.Hóa trị cisplatin thường xuyên hơn (ví dụ: hàng tuần hoặc hàng ngày) được yêu cầu để tăng độ nhạy cảm. Một thử nghiệm ngẫu nhiên về hóa chất tân bổ trợ cisplatin và 5-FU sau đó xạ trị so với hóa xạ đồng thời với cisplatin và 5-FU ở bệnh nhân ung thư đầu và cổ không thể phẫu thuật cho thấy tỷ lệ sống tương tự nhưng khả năng kiểm soát tại chỗ cho nhóm hóa xạ đồng thời được cải thiện hơn. Các kết quả đã được trình bày cho bệnh nhân ung thư có thể cắt bỏ giai đoạn II đến IV, khi so sánh một phác đồ tân bổ trợ ba chu kỳ taxane sau đó là hóa xạ đồng thời hàng tuần với carboplatin (hoặc xạ trị tăng cường gia tốc với Docetaxel hàng tuần) rồi hóa- xạ trị đồng thời tăng cường gia tốc với cisplatin cứ sau 21 ngày. Thử nghiệm pha III này cho thấy không có sự khác biệt về thời gian sống còn trong 3 năm. Một thử nghiệm pha II, so sánh hóa xạ trị đồng thời với docetaxel hoặc 5FU và hydroxyurea, cả hai được hóa trị mỗi tuần có hoặc không có hóa trị tân bổ trợ ba chu kỳ với taxanes, cho thấy thời gian sống sót không bệnh tốt hơn nhưng thời gian sống còn toàn bộ là tương tự cho nhóm hóa trị tân bổ trợ. Do đó, hóa xạ đồng thời với platinum có thể được xem xét cho bệnh nhân ung thư đầu và cổ tiến triển có chỉ số hoạt động cơ thể tốt.

Phác đồ hóa xạ đồng thời sử dụng taxan với 5-FU hoặc cisplatin cho thấy những kết quả đầy hứa hẹn cũng như các phác đồ có chứa 5-FU và hydroxyurea với xạ trị hai lần mỗi ngày, cùng với hóa trị đồng thời mỗi tuần. Các tác nhân ức chế tín hiệu EGFR đã được đánh giá là chất tăng cường bức xạ trong ung thư vảy ở đầu và cổ. Hơn 90% ung thư vảy ở đầu và cổ biểu hiện EGFR(+), và biểu hiện này gia tăng có mối tương quan với tỷ lệ sống còn kém hơn sau xạ trị. Các kháng thể đơn dòng ức chế EGFR cetuximab đã được chứng minh là tăng cường đáp ứng và thời gian sống còn chỉ cần nhờ xạ trị đơn độc, mặc dù hơn 50% số người tham gia thử nghiệm có khối u nguyên phát ở hầu họng, một loại trước đây đã đáp ứng cao với xạ trị. Ngược lại với các thử nghiệm khi so sánh xạ trị có hoặc không có hóa trị, không giảm di căn xa trong nhóm cetuximab. Các nghiên cứu lâm sàng đang được tiến hành với sự kết hợp của các chất ức chế EGFR, với xạ trị và với các tác nhân hóa trị tiêu chuẩn. Các báo cáo sơ bộ của RTOG 0522 cho thấy không có lợi ích về thời gian sống còn hoặc thời gian bệnh không tiến triển với việc bổ sung cetuximab vào hóa trị cisplatin tiêu chuẩn. Sau khi hóa trị ở bệnh nhân có N2, N3 hoặc nhiều hạch khi chẩn đoán, phẫu thuật nạo vét hạch chọn lọc có thể được tiến hành khi có đáp ứng hoàn toàn tại vị trí u nguyên phát, đặc biệt là khi đáp ứng tại hạch không hoàn toàn sau hóa trị. Phẫu thuật cứu vớt có thể được tiến hành nếu không đạt được sự kiểm soát hoàn toàn tại vị trí u chính.
Theo: “The Bethesda Handbook of Clinical Oncology, 4th Edition”
- 09/06/2019 08:51 - Xét nghiệm chức năng tuyến giáp và mang thai
- 05/06/2019 17:59 - Ung thư vú (phần 1)
- 19/05/2019 14:50 - Hội chứng đột quỵ - tim
- 19/05/2019 14:27 - Tiếp cận thai nghén thất bại sớm
- 14/05/2019 17:21 - Sử dụng thuốc chống loạn nhịp trong và ngay sau kh…
- 07/05/2019 12:14 - Xét nghiệm sàng lọc máu
- 07/05/2019 11:59 - Ung thư tuyến giáp (p.1)
- 25/04/2019 21:00 - Viêm dạ dày tự miễn
- 20/04/2019 10:56 - Ascorbic acid, corticosteroids và thiamine trong n…
- 19/04/2019 19:00 - Điều trị nhiễm khuẩn huyết liên quan đến đường tru…
